第二章
縮合リン酸塩
無機リン酸塩には、
オルトリン酸(一般的にリン酸)と縮合リン酸、低級リン酸に大別される。
今回は、縮合リン酸塩を中心に説明する。
縮合リン酸塩とは
縮合リン酸塩とは、オルトリン酸(H3PO4)を加熱することにより脱水反応が起こり、無機高分子となった物の総称である。たとえば、
ナトリウム塩
2Na2HPO4 →Na4P2O7(ピロリン酸四ナトリウム)+H2O(190℃付近)
2NaH2PO4 →Na2H2P2O7(ピロリン酸二水素二ナトリウム)+H2O(190℃付近)
Na2H2P2O7 →NaPO3(メタリン酸ナトリウム)(260℃以上)
カルシウム塩
Ca(H2PO4)2 → γ-Ca(PO3)2(メタリン酸カルシウム:350℃) →β-Ca(PO3)2(600℃) → α-Ca(PO3)2 (970℃)
CaHPO4 → γ-CaP2O7(ピロリン酸カルシウム:320~340℃) →β-CaP2O7(700~750℃) → α-CaP2O7(1140℃)
など加熱温度により生成される物質が異なる。
重合リン酸塩の金属イオン封鎖
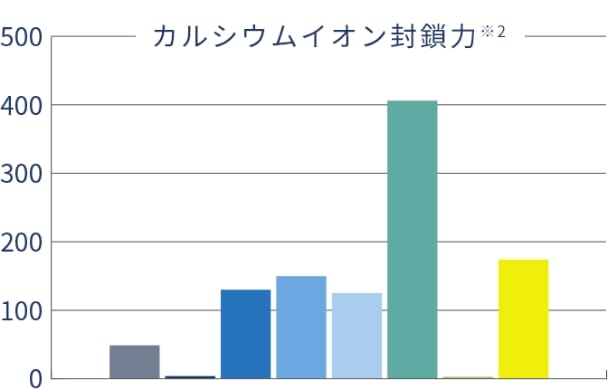
キレート剤(別名)
- ピロリン酸ナトリウム(無水)(ピロリン酸四ナトリウム(無水))
- 酸性ピロリン酸ナトリウム(ピロリン酸二水素二ナトリウム)
- トリポリリン酸ナトリウム(ポリリン酸ナトリウム)
- テトラポリリン酸ナトリウム(ポリリン酸ナトリウム)
- メタリン酸ナトリウム(ヘキサメタリン酸ナトリウム)
- ウルトラポリン(ウルトラリン酸ナトリウム)
- クエン酸
- フィチン酸
【図2】重合リン酸塩の金属イオン封鎖
これら縮合リン酸塩には、ポリリン酸塩、メタリン酸塩とウルトラリン酸があり、金属とリンの原子比率Me2O/P2O5(以降Rと表記:Meは一価の金属として計算)によって分類される。ポリリン酸塩は2>=R>1、メタリン酸塩はR=1、ウルトラリン酸塩はR<1の範囲とされている。
これらは構造的な違いがあり、ポリリン酸はPO4四面体がP-O-Pで鎖状に連結、メタリン酸はPO4四面体がP-O-Pで環状に連結され、ウルトラリン酸は網目状に連結された無機高分子である。(「ヘキサメタリン酸ナトリウム」は一般名称であり、ここで言う環状構造では無く、鎖状構造の高分子量体が多く含まれている)
※注:数値は、社内データです。実験方法の性質上、数値は測定条件等で変わりますので、本表内での相対値として参照してください。
※注:Caイオンの封鎖性を検討する方法にはいろいろありますが、もっとも多く利用されているのが、 Dow Chem. 法によりChelation Value (C. V.)を求める方法です。数値が大きいほど、封鎖力が強いです。